作为典型的柔性材料,凝胶材料因具有良好的粘弹性,透明性,生物相容性以及与人体软组织类似的结构和性能而在细胞治疗,生物传感器,组织工程等生物医学领域以及柔性电子和柔性机器等工程技术领域具有重要科学意义和广阔的应用前景。由于其特殊的使用要求,需对其力学性能、生物相容性、功能化等进行设计调控,以满足在不同领域中的需求。
西安交通大学陈咏梅课题组近年来逐步建立了一系列成熟的多功能凝胶材料合成及结构性能调控的方法,并且围绕自愈合性能、磁学性能、发光性能、导电性能,高机械性能等,开发了一系列多功能凝胶材料(图1),展示了其在三维细胞包埋、磁性导管、柔性透明可拉伸导线和柔性器件等方面的优异性能,为生物医学研究和柔性器件的发展提供了新手段和新技术。

图1 陈咏梅教授课题组研发的多功能水凝胶材料
1. 可在生理环境下自愈合的多糖水凝胶
作为一种新型智能材料,自愈合凝胶在解决软材料损伤修复问题,实现柔性材料智能化和高效化方面具有重要意义。陈咏梅课题组研制了基于天然多糖的可在生理条件下自愈合,并且具有良好细胞相容性的新型自愈合水凝胶材料。这些具有优异性能的水凝胶材料有望作为细胞或药物载体应用于生物医学领域。合成了基于动态共价化学的多糖基自愈合水凝胶,该水凝胶中含有酰腙键和亚胺键两种动态共价化学键,是通过己二酰肼(adipic acid dihydrazide,ADH)交联氧化海藻酸钠(oxidizedsodium alginate, OSA)生成可逆酰腙键,同时通过氧化海藻酸钠交联水溶性壳聚糖(N-carboxyethylchitosan,CEC)得到可逆亚胺键来形成基于两种动态共价化学键的多糖基自愈合水凝胶材料,称为CEC-l-OSA-l-ADH 水凝胶(“l” 表示 “交联”),该水凝胶在生理条件下具有较高的自愈合效率,值得一提的是该水凝胶还有可注射性和降解性能。上述优势赋予该水凝胶三维包埋和释放活体细胞的功能(Adv.Funct.Mater.2015, 25(9):1352-1359封底论文)(图2a)。
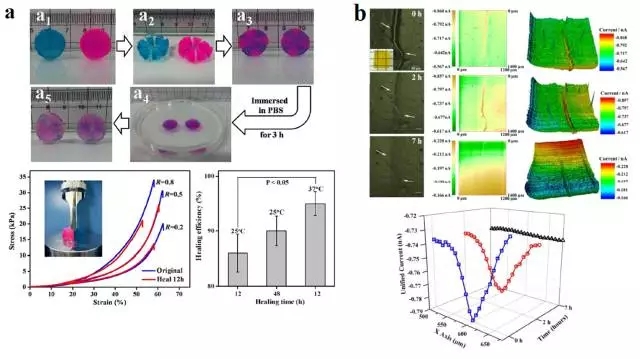
图2. 多糖基自愈合水凝胶。(a)CEC-l-OSA-l-ADH在生理环境下自愈合照片;自愈合力学性能测试;外界环境对自愈合性能的影响。(b)SECM检测葡聚糖自愈合水凝胶的自愈合过程和效率。
此外,还提出了一种基于可逆迪尔斯-阿尔德(DA)反应的天然多糖自愈合水凝胶的合成制备方法。以修饰有富烯基团的葡聚糖(fulvene-modified dextran,Dex-FE)为双烯体,二氯马来酸修饰的聚乙二醇(PEG-dichloromaleic anhydride,PEG-DiCMA)为亲双烯体制备了自愈合水凝胶材料,研制出了可在生理条件下自愈合,并且具有良好细胞相容性的葡聚糖自愈合水凝胶。Dex-FE与PEG-DiCMA在37°C下,pH7.0的磷酸盐缓冲溶液(PBS)中发生可逆DA反应交联制备得到葡聚糖自愈合Dex-l-PEG水凝胶。首次采用扫描电化学显微镜(SECM)对水凝胶自愈合过程进行了三维实时监测(Macromol.Rapid Comm. 2013, 34 (18): 1464-1470)(图2b)。并受邀在化学领域权威综述刊物Chem.Soc. Rev. (2014, 43 (23): 8114-8131)上发表了自愈合凝胶材料的设计合成及其在生物医学和工程技术领域的综述,展望了未来发展方向。
2. 高强度水凝胶材料
传统高分子水凝胶材料因力学性能低而难以实现其实际应用。高强度水凝胶材料的设计对大幅度提高水凝胶力学性能以及推动功能水凝胶材料在生物材料和柔性器件中的应用研究意义重大。陈咏梅课题组与哈佛大学锁志刚教授合作,通过简便的两步法可制备得到具有高度可拉伸性能的高强度海藻酸钠(alginate)/聚丙烯酰胺(PAAm)复合水凝胶,并在此设计思路上制备了具有抗撕裂功能的高强度磁性水凝胶材料。不同二价离子(Ca2+,Sr2+, Ba2+)和三价离子(Al3+,Fe3+)对海藻酸钠的交联显著影响水凝胶的力学性能。拉伸测试表明三价阳离子交联的水凝胶的断裂应力高达~900kPa,能量耗散高达~2000kJ×m−3。此外,该水凝胶薄片可以吹成一个大气球,60秒时其面积变化为760%,进一步证实了其优异的力学性能(图 3)(ACS Appl. Mater.Interfaces.2013,5(21):10418-10422)。
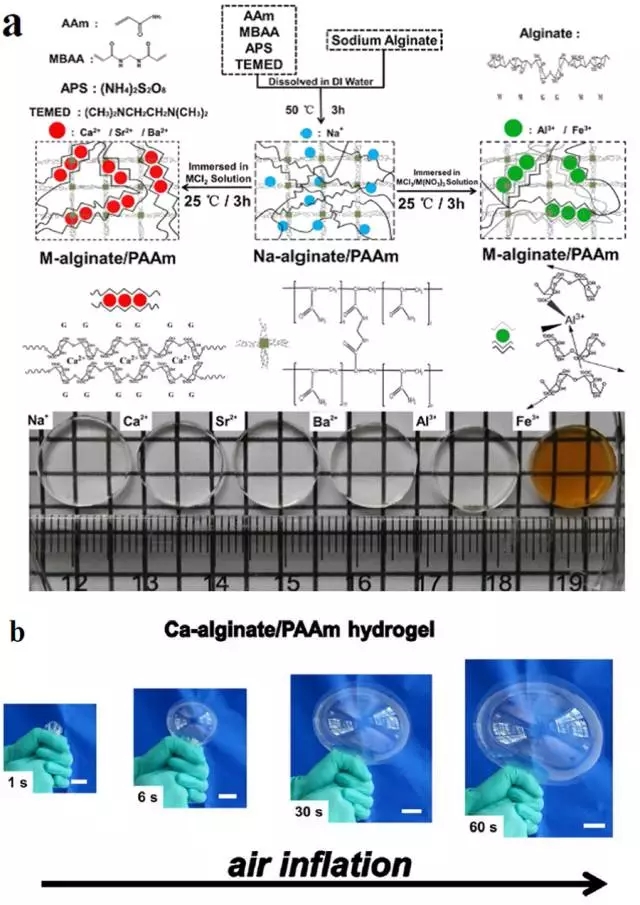
图3 两步法制备不同离子交联的alginate/PAAm复合水凝胶流程图(a),以及水凝胶吹气球过程照片(b)(比例尺: 4 mm)。
3.抗撕裂性能的高强度磁性水凝胶材料
针对目前大部分磁性水凝胶的机械性能差,不能满足荷载承力柔性器件需求的现状,陈咏梅课题组首次设计制备了具有抗撕裂性能的高强度磁性水凝胶材料。在高强度海藻酸盐/聚丙烯酰胺水凝胶中适量均匀掺杂经海藻酸钠修饰的磁性Fe3O4纳米粒子,发现水凝胶不但具有良好的磁响应性能,而且具有良好的力学性能和抗撕裂性能,压缩强度可高达~5MPa,拉伸强度可高达~1MPa,且拉伸长度可达~10倍,打结、弯曲该磁性水凝胶也能保持其良好的状态(图4),断裂能高达~1600-3000 J m-2。即使带有预切口的水凝胶材料,拉伸长度也可达8.8倍(图5)。并进一步展示了高强度磁性水凝胶作为悬臂梁弯曲致动器和磁性微创医疗导管材料的初步应用。该研究结果为在赋予水凝胶磁响应性的同时保证其高力学性能,拓展磁性水凝胶材料的应用领域奠定了基础。

图4 (a)高强度海藻酸盐/聚丙烯酰胺水凝胶结构示意图,以及(b) 水凝胶拉伸、压缩、打结照片, (c)水凝胶在磁场驱动下的响应性。比例尺: 1 cm.
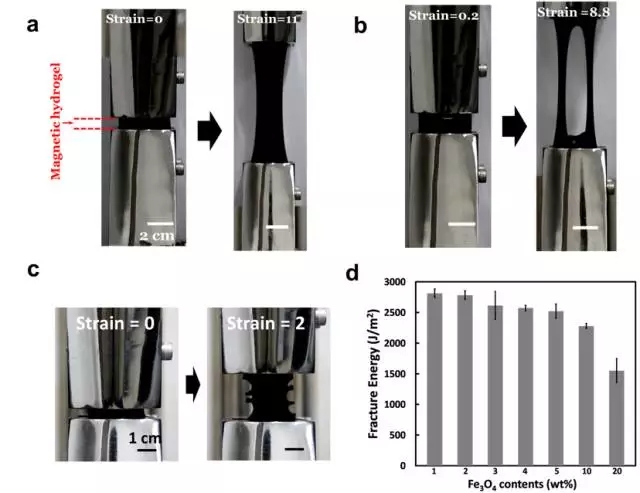
图5 (a)高强度磁性水凝胶拉伸照片;(b) 带有中间预切口的高强度磁性水凝胶拉伸照片;(c) 带有多个预切口的高强度磁性水凝胶拉伸照片; (d) 磁性水凝胶断裂能.
4.高强度温敏水凝胶材料
针对目前大部分温度敏感型水凝胶的机械性能差,响应速率慢,不能满足荷载承力柔性器件需求的现状,陈咏梅课题组首次设计制备了具有高力学性能、快速响应且相转变温度可调节的温敏水凝胶材料。该水凝胶由海藻酸铝/聚N-异丙基丙烯酰胺构建互穿网络,其中离子交联的海藻酸铝作为牺牲键在凝胶网络体系中耗散能量以避免应力集中,低交联的聚N-异丙基丙烯酰胺网络赋予凝胶网络良好的弹性,两层网络协同作用增强水凝胶力学性能。制备所得水凝胶压缩强度高达~6MPa,拉伸强度最高达~350kPa,且拉伸倍率可达~10倍。与此同时,水凝胶体系中存在大量的盐离子能够降低聚N-异丙基丙烯酰胺的相转变温度,调节盐离子的浓度可实现该水凝胶相转变温度的可控调节性。随盐离子浓度由0.1mol/L逐渐增大至0.7mol/L,水凝胶相转变温度由32°C降低至22.5°C。因此,在此基础上构建了一种低温快速响应的水凝胶驱动器,该驱动器在30°C水环境中40s内迅速达到~140°的弯曲角度,由驱动器构建的柔性机器抓手可在水中快速抓取物体(图6)。该研究结果为高强度温敏水凝胶材料的设计及其在柔性机械方面的应用提供了很好的借鉴作用及理论基础。
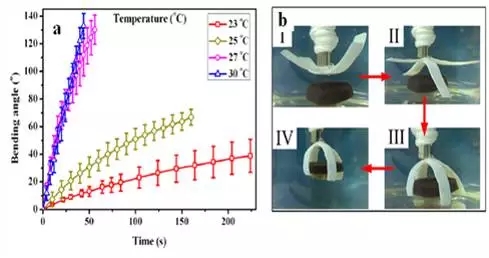
图6 海藻酸铝/聚N-异丙基丙烯酰胺水凝胶驱动器在不同环境温度中弯曲角度随时间的关系(a)及在水中抓取物体过程照片(b)。
5.发光水凝胶
光致发光凝胶材料已经成为应用于生物成像、药物输送、传感器、光开关等许多领域的新型柔性材料。陈咏梅课题组将铱金属配合物以及镧系元素引入水凝胶中,制备了具有优良发光性能和细胞相容性的发光水凝胶材料。首先提出了一种通过简便的扩散法制备得到基于阳离子型铱金属配合物[Ir(ppy)2(dmbpy)]Cl和带负电荷的水凝胶的新型发光水凝胶的制备方法。带负电荷的水凝胶与带正电荷的 [Ir(ppy)2(dmbpy)]Cl之间强的静电相互作用促进了磷光分子在水凝胶网络中的扩散,并形成了稳定的复合材料,即使在水中浸泡9个月水凝胶也具有良好的发光性能(图7)(Macromol. Rapid Commun. 2012, 33, 1191-1196,封面论文)。
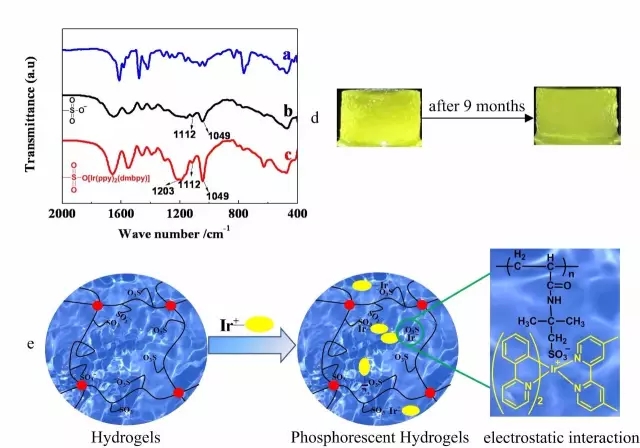
图 7 (a),(b),(c)[Ir(ppy)2(dmbpy)]Cl粉末的红外光谱, (d) Eq–IrIII–PNaAMPS水凝胶浸泡9个月前后的磷光照片,(e) PNaAMPS水凝胶和 [Ir(ppy)2(dmbpy)]Cl分子之间相互静电作用的示意图(红点:交联点, 黄点: [Ir(ppy)2(dmbpy)]Cl
然而,传统发光水凝胶因机械性能较低而严重限制了其应用范围。针对该问题,陈咏梅课题组设计了高力学性能的发光水凝胶,镧系元素-海藻酸钠/聚丙烯酰胺复合水凝胶材料。其中镧系元素作为发光元素和物理交联剂引入复合水凝胶中。该水凝胶具有多功能的优点,包括良好的发光性能,颜色可以通过采用不同的镧系元素而调节,并可以根据实际应用需要制备成不同的形状,可承受较大力学变形,良好的加工性能和细胞相容性,兆帕级抗压强度、约20倍拉伸变形及高能量耗散(~9000 kJ m−3)(图8)(Macromol. Rapid Commun. 2015, 36, 465−471)。上述制备复合发光水凝胶的方法具备以下优势:(1)制备过程相对简便;(2)水凝胶和发光材料组合具有多样性;(3)发光材料的分子结构和性能在水凝胶网络中得到保存,使发光材料的发光性能实现最大化。新型光致发光水凝胶有望拓宽水凝胶的使用范围。
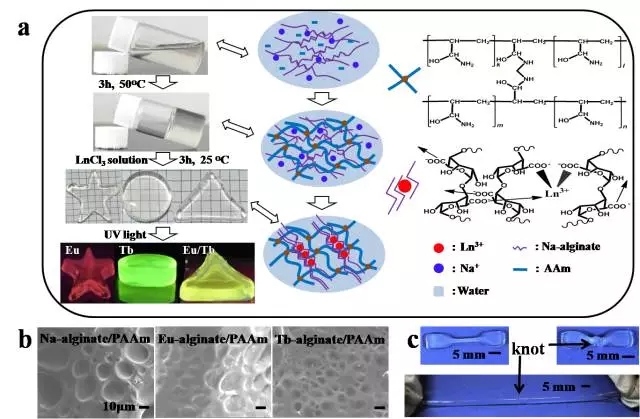
图 8 (a) 高强度发光水凝胶制备过程;(b) 高强度发光水凝胶SEM照片;(c) 高强度发光水凝胶打结、拉伸变形照片。
6.水凝胶调控磁性纳米粒子晶体生长
针对水热法、高温分解法等方法虽可制备形貌可控的Fe3O4纳米粒子,但因使用有毒试剂和有机溶剂易对环境造成很大污染,且需要高温高压等苛刻反应条件,不利于产物大规模制备以及在生物医学环境等领域中的应用等问题。陈咏梅课题组借鉴趋磁细菌利用其磁小体囊泡内带负电荷的蛋白质作为吸附富集铁离子的位点,并将磁小体囊泡做为微反应器,在其体内原位合成出形貌高度可控的磁性纳米粒子,以水凝胶三维网络结构作为模拟趋磁细菌中合成Fe3O4纳米晶体的微环境,首次实现了通过简单温和的共沉淀反应在水凝胶体系中原位制备得到负载一系列规则形貌的Fe3O4纳米粒子的磁性水凝胶,并发现了水凝胶内部微环境调控Fe3O4纳米粒子晶体生长的机理(Green Chem.2014, 16:1255-1261;ChemPhysChem.2016, DOI: 10.1002/cphc.201600117)。该制备过程采用无毒性的试剂以及廉价的Fe2+与Fe3+作为前驱体,操作简单,避免了引入表面活性剂等影响生物材料细胞相容性的成分。SEM图像中可以清楚地观察到水凝胶内原位生成的Fe3O4纳米粒子可具有规则的八面体,纳米棒及纳米针等形貌,高分辨TEM图像可清楚的观察到单个典型的Fe3O4纳米粒子的几何结构,分别为表面暴露{111}晶面的Fe3O4纳米八面体以及沿着[211]晶向生长的Fe3O4纳米棒及纳米针(图9)。此外,负载于水凝胶中的Fe3O4纳米粒子仍然具有良好的拟过氧化物酶活性,不仅可用于检测微量的过氧化氢,而且可作为新型高效污水处理材料实现阳离子型染料的快速降解处理。

图9 原位制备负载一系列规则形貌Fe3O4纳米粒子的磁性水凝胶流程图,水凝胶网络中Fe3O4纳米粒子的SEM图像和单个Fe3O4纳米粒子的高分辨TEM图像。
7.细胞培养支架
高分子水凝胶是一种透明或半透明的软、湿生物材料,因其含水量高(~90%),具有与生物体软组织相似的模量(~kPa),内部的三维网络结构有利于营养物质及代谢废物的扩散,具有与细胞外基质相似的结构和性能,是一种良好的细胞培养支架材料。细胞在体外扩增、培养过程中所需支架材料作为组织工程中极其重要的一个组成部分,不仅关系到经扩增得到的细胞数目是否能满足需求,而且还显著影响细胞功能,因此,如何选择合适的材料作为培养支架进行体外细胞培养扩增是亟需解决的问题。为了解决人体视网膜色素上皮细胞(retinal pigment epithelium, RPE)在体外培养时易于老化的问题,陈咏梅课题组开展了在高分子水凝胶支架表面培养RPE细胞的工作,并研究了水凝胶性能对RPE细胞氧化应激性能的影响。发现带负电荷的水凝胶可以促进ARPE-19细胞扩增,并通过对细胞核和细胞骨架蛋白(F-actin)的染色表明细胞扩增生长为密集的细胞单层膜。通过测定不同弹性模量的水凝胶表面培养的ARPE-19细胞膜的活性氧簇(reactive oxygen species, ROS)发现,水凝胶的弹性模量显著影响细胞的ROS。当水凝胶的弹性模量分别为5.0kPa和24.0kPa时,比在组织培养板表面培养的细胞的ROS分别低44%和50%,然而当水凝胶的弹性模量为169.3kPa时,与在组织培养板表面培养的细胞的ROS没有显着性差异(图10)。可以推测低模量的水凝胶为ARPE-19细胞提供了更类似于其在体内的生长微环境,有助于细胞增强其固有的抗氧化防御功能(J. Biomed.Mater. Res. A 2014,102A: 2258-2267)。
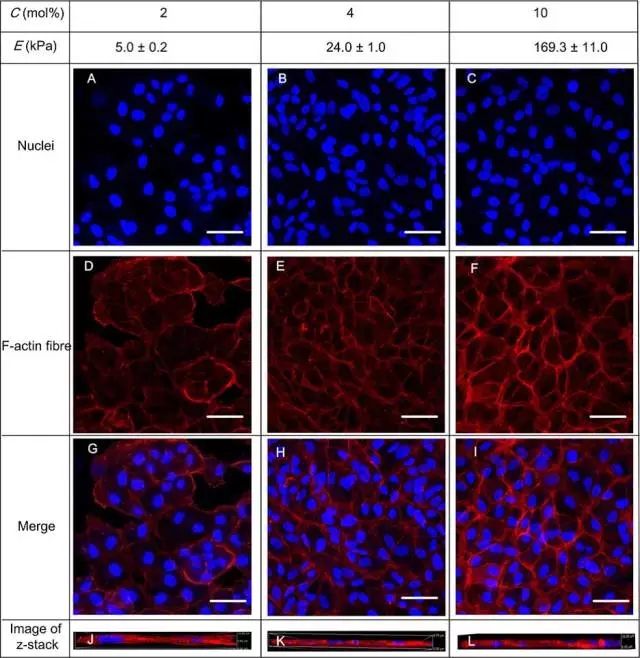
图10 不同杨氏模量的水凝胶表面的RPE 细胞培养120h 后的形态。(a)、(b)、(c):由DAPI 染色的细胞核。(d)、(e)、(f):由罗丹明鬼笔环肽染色的F-actin。(g)、(h)、(i):将细胞核及F-actin 染色叠加之后的结果。(j)、(k)、(l):水凝胶表面培养细胞的纵剖面图。(标尺:100μm)
与二维培养体系相比,三维包埋细胞培养体系可以更好的模拟体内的微环境,利于实现细胞与细胞之间、细胞与基质之间的相互作用,从而使培养的细胞具有与体内相似的环境,因此在生物医药领域得到了广泛使用。原位成型水凝胶可以在形成水凝胶的过程中直接包埋细胞,从而实现细胞的均匀包埋,并且可以按照需求制备出各种复杂的形状,这些特性使得它广泛应用于三维细胞包埋。然而,目前常规使用的原位成胶方法中,经常使用会产生细胞毒性的试剂(引发剂)及方法(紫外光,加热),限制了它们在三维包埋中的应用。巯基-迈克尔加成反应是一种具有高选择性、高反应效率的点击化学反应,并且可以在生理条件下进行反应,这些特点使得其在制备三维水凝胶支架材料方面很有竞争力。陈咏梅课题组在生理条件下采用巯基-迈克尔加成反应,利用甲基丙烯酸缩水甘油酯修饰的葡聚糖(Dex-GMA)与二硫苏糖醇(DTT)在生理环境下交联制备得到了葡聚糖基水凝胶Dex-l-DTT。该凝胶的形成过程、力学强度、溶胀率及凝胶的微观网络结构均可以通过改变pH(7.0-7.8)而调节。使用该水凝胶体系,成功的实现了纤维细胞(NIH-3T3)及小鼠骨髓间充质干细胞(BMSCs)的三维包埋,并且包埋的细胞均保持了较高的活性,证明了水凝胶良好的细胞相容性。碱性磷酸酶染色(ALP)活性检测表明了包埋的干细胞不仅保持了较高的活性,而且还具有分化能力(图11)。易于调节的凝胶性质及良好的细胞相容性证明了Dex-l-DTT水凝胶作为细胞三维培养支架材料的应用潜力(Colloids Surf.B Biointerfaces, 2015, 128: 140-148)。基于上述研究基础我们提出:作为组织工程用细胞培养支架材料,仅仅能促进细胞的生长还远远不够,只有在其中培养的细胞具备与体内细胞同样功能的材料,才在组织工程中具有应用价值的学术观点。

图11 巯基-迈克尔加成反应制备Dex-l-DTT 水凝胶的过程示意图和照片,细胞包埋过程示意图以及包埋的BMSCs 分别培养在成骨培养液(OS)与普通培养液(Control)1, 3, 5, 7, 9 ,14 d 后的ALP 表达量。
8.水凝胶导线
在新型功能凝胶材料的设计制备方面,具有高拉伸性能柔性离子导电材料因可为任意弯曲,拉伸,压缩,扭曲的柔性电子(flexible electronics)器件在变形为复杂的、非平面形状的同时,保持良好的使用性能,可靠性和集成性提供关键技术储备而得到了广泛关注。陈咏梅课题组与哈佛大学锁志刚教授合作,成功制备了同时具有良好导电性能、高拉伸性能、透明度高、并且电阻不随应变而显著变化的柔性离子导体(含有盐的水凝胶和离子液体凝胶)及柔性器件。制备了具有良好拉伸性能、低弹性模量、良好导电性、高透明度、稳定性于一体的导电水凝胶和离子液体凝胶材料。采用导电水凝胶研制了柔性透明可拉伸导线,可代替耳机线播放音乐,即使拉伸十倍以上也可正常播放音乐(图12)(ExtremeMechanics Letters 2015,3: 59–65)

图12 透明可拉伸水凝胶导线。
参考文献:
[1] WeiZ, Yang JH, Zhou JX, Xu F, Zrínyi M, Dussault PH, Osada Y, Chen YM,Self-Healing gels based on constitutional dynamic chemistry and their potentialapplications, Chem. Soc. Rev. 2014, 43 (23): 8114 – 8131
[2] WeiZ, Yang JH, Liu ZQ, Xu F, Zhou JX , Zrínyi M, Osada Y, Chen YM, Novel biocompatible polysaccharide-basedself-healing hydrogel, Adv. Funct. Mater. 2015, 25(9):1352–1359 (inside cover)
[3] WeiZ, Yang JH, Du XJ, Xu F, Zrinyi M, Osada Y, Li F, Chen YM. Dextran-basedself-healing hydrogels formed by reversible diels-alder reaction underphysiological conditions. Macromol. Rapid Comm. 2013, 34 (18): 1464-1470(coverpaper)
[4] YangCH, Wang MX, Haider H, Yang JH, Sun JY, Chen YM, Zhou JX, Suo ZG. Strengtheningalginate/polyacrylamide hydrogels using various multivalent cations. ACS Appl.Mater. Inter. 2013, 5: 10418-10422
[5] Haider H, Yang CH,Zheng WJ, Yang JH, Wang MX, Yang S, Zrinyi M, Osada Y, Suo Z, Zhang Q, Zhou J,Chen YM, Exceptionally tough and notch-insensitive magnetic hydrogels, SoftMatter, 2015,11,42,8253–8261
[6] Wang MX, Yang CH, Liu ZQ, Zhou J, Xu F, Suo Z,Yang JH, Chen YM. Tough photoluminescenthydrogels dopedwith lanthanide. Macror Rapid Commun 2015, 36 (5): 465-471
[7] ZhengWJ, An N, Yang JH, Zhou JX, Chen YM. Tough Al-alginate/Poly(N-isopropylacrylamide) hydrogel with tunable LCST for soft robotics. ACS Appl. Mater.Interfaces 2015, 7 (3): 1758-1764
[8] GaoY, Wei Z, Li F, Zrínyi M, Osada Y, Yang ZM, Chen YM. Synthesis of morphologycontrollable Fe3O4 nanoparticles/hydrogel magneticnanocomposite inspired by magnetotactic bacteria and its application in H2O2detection. Green Chem. 2014, 16 (3): 1255-1261
[9] ChenYM, Liu ZQ, Feng ZH, Xu F, Liu JK. Adhesive protein-free synthetic hydrogelsfor retinal pigment epithelium cell culture with low ROS level. J. Biomed.Mater. Res. A 2014, 102 (7): 2258–2267
[10] LiuZQ, Wei Z, Zhu XL, Huang GY, Xu F, Yang JH, Osada Y, Zrínyi M, Li JH, Chen YM,Dextran-based hydrogel formed by thiol-Michael addition reactionfor 3D cellencapsulation, Colloids Surf. B Biointerfaces, 2015,128,140–148
[11] YangCH, Chen B, Lu JJ, Yang JH, Zhou J, Yong Mei Chen YM, Suo Z. Ionic cable,Extreme Mechanics Letters 2015,3, 59–65
[12] ChenBH, Lu JJ, Yang CH, Yang JH, Zhou JX, Chen YM, Suo ZG, Highly stretchable andtransparent ionogels as nonvolatile conductors for dielectric elastomertransducers, ACS Appl. Mater. Inter. 2014, 6 (10): 7840−7845



